
Ai infertilitate?
Infertilitatea reprezintă imposibilitatea de a concepe un copil după cel puțin un an de contact sexual neprotejat. În România, investigațiile încep de obicei cu femeia, considerată frecvent cauza, însă adesea se constată ulterior că aceasta este sănătoasă, iar problema este depistată la bărbat printr-o simplă spermogramă. Deoarece investigațiile masculine sunt mai rapide și mai puțin complexe, se recomandă ca, în cazul infertilității de cuplu, bărbatul să fie primul evaluat medical.
Mai jos găsești răspunsuri la probleme medicale frecvent întâlnite. Dacă dorești mai multe informații sau nu ai găsit un răspuns, te rugăm să ne contactezi sau să ne trimiți un mesaj prin pagina noastră de contact.

Infertilitatea este imposibilitatea de a concepe un copil după cel puțin un an de contact sexual neprotejat.
În România, atunci când un cuplu nu poate concepe copii, investigația medicală începe, de regulă, cu femeia, aceasta fiind considerată cel mai adesea cauza infertilității.
După investigații multiple și complexe, care pot dura ani, se constată frecvent că femeia este sănătoasă. Abia ulterior bărbatul efectuează o spermogramă, care poate evidenția cauza infertilității (de exemplu, absența spermatozoizilor din spermă).
Investigațiile pentru bărbat sunt mai simple, mai rapide și mai puțin invazive, ceea ce permite stabilirea mai rapidă a diagnosticului și inițierea tratamentului. De aceea, în cazul infertilității de cuplu, recomandarea este ca bărbatul să fie investigat primul prin spermogramă, iar dacă rezultatul este normal, să se continue evaluarea femeii.
În România nu există studii recente privind prevalența infertilității generale și masculine. Studiile internaționale arată însă că în 6 din 10 cupluri infertile cauza este parțial sau total masculină.
Infertilitatea masculină apare la toate grupele de vârstă, dar majoritatea bărbaților se prezintă la medic după 30 de ani. Doar aproximativ 1 din 10 bărbați sub 30 de ani consultă un urolog pentru această problemă.
Mulți nu înțeleg că tratarea tardivă scade șansele de succes. Cei mai mulți ajung la medic când nu pot avea un copil, când descoperă un varicocel la palpare sau când au o boală cu transmitere sexuală.
În Europa de Vest, după un an de activitate sexuală neprotejată fără obținerea unei sarcini, primul investigat este bărbatul, deoarece evaluarea este mai ușoară, neinvazivă și rapidă.
Un bărbat este considerat 100% infertil când are 0 spermatozoizi în spermogramă. Dacă are un număr scăzut, cu mobilitate și morfologie deficitare, este diagnosticat ca subfertil.

Examenul clinic
Examinarea este realizată de medicul urolog și se concentrează pe organele genitale externe: penis și scrot (cu examinarea atentă a testiculelor). Se pot identifica varicocelul, testiculul necoborât, absența ductului deferent sau alte anomalii de dezvoltare.
Examenul scrotului: se evaluează tegumentul, infecțiile, consistența, mobilitatea planurilor și sensibilitatea. Testiculul normal are aproximativ 5 cm diametru, formă ovoidală, consistență fermă, neted și nedureros.
Testiculele mici și moi asociate cu spermogramă deficitară sugerează afectarea spermatogenezei. Testicul normal la examen, dar cu spermogramă scăzută, poate indica patologie obstructivă. Se poate efectua termografie scrotală.
Varicocelul: când este vizibil sau palpabil fără manevre speciale, asociază frecvent infertilitate. Vasele dilatate au consistența descrisă clasic ca „pachet de rame”. Uneori dispare la decubit dorsal, motiv pentru care examenul trebuie realizat atât culcat, cât și în ortostatism, inclusiv cu manevra Valsalva.
Examinarea penisului: se inspectează tegumentul, se decalotează pentru depistarea ulceratiilor, balanitelor, cicatricilor post-sancru sifilitic, se palpează uretra și se verifică meatul urinar pentru scurgeri.
Tuseul rectal: etapă obligatorie pentru evaluarea prostatei (dimensiuni, consistență, simetrie, omogenitate, temperatură, sensibilitate). Prostata este dureroasă și fierbinte în prostatită acută, cu consistență crescută în cancer și volum modificat în hipertrofia benignă.
Anamneza
Pacientul trebuie să prezinte corect antecedentele patologice, fiziologice, heredocolaterale și istoricul vieții sexuale. Sunt relevante:
- frecvența actului sexual
- boli cu transmitere sexuală în antecedente
- durata infertilității și eventuale concepții anterioare
- modificări ale caracterelor sexuale secundare
- boli grave (cancer, infecții respiratorii, intervenții genitale)
- expuneri la toxice și radiații
- alergii
- probleme de fertilitate în familie
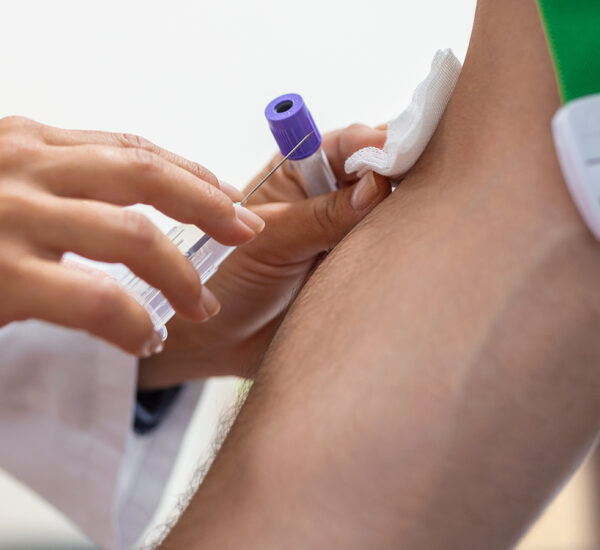
Analize sanguine
Pe lângă hemoleucogramă, glicemie și biochimie, se efectuează determinări hormonale.
Dacă spermograma indică sub 10 milioane/ml, se dozează testosteron și FSH. Dacă testosteronul este scăzut, se investighează LH. Valori normale: FSH 2–15 UI/L; testosteron 30–100 ng/ml.
Valori scăzute sugerează hipogonadism hipogonadotrop. FSH foarte crescut indică afectare primară a spermatogenezei (absența celulelor Sertoli sau leziuni ale tubilor seminiferi).
Se pot determina prolactina, estrogenii, adrenalina în caz de libido scăzut sau ginecomastie. Se efectuează și teste pentru depistarea infecțiilor.
Testul postcoital (Sinus-Huhner)
Evaluează capacitatea spermatozoizilor de a penetra mucusul cervical. Se efectuează în perioada ovulatorie, la 2–24 ore după contact sexual. Mucusul este analizat microscopic. Lipsa spermatozoizilor vii impune teste suplimentare pentru infecții sau cauze imunologice. Testul nu evaluează capacitatea de fecundare și este mai rar utilizat în prezent.
Ecografia testiculară
Metodă imagistică accesibilă pentru evaluarea dimensiunilor (normal: 4,5 cm, volum ~20 ml), chisturi, tumori, varicocel incipient. Nu stabilește diagnosticul de cancer și depinde de experiența examinatorului.
Teste genetice
Indicate în spermograme sever modificate fără obstrucție sau în cazuri de ICSI. Aproximativ 1/3 dintre bărbații incluși în programe de reproducere asistată prezintă defecte genetice. Se analizează posibilitatea utilizării diagnosticului genetic preimplantare pentru detectarea anomaliilor (fibroză chistică, distrofie musculară, talasemii).
Testarea genetică poate fi un predictor mai important decât simpla spermogramă.
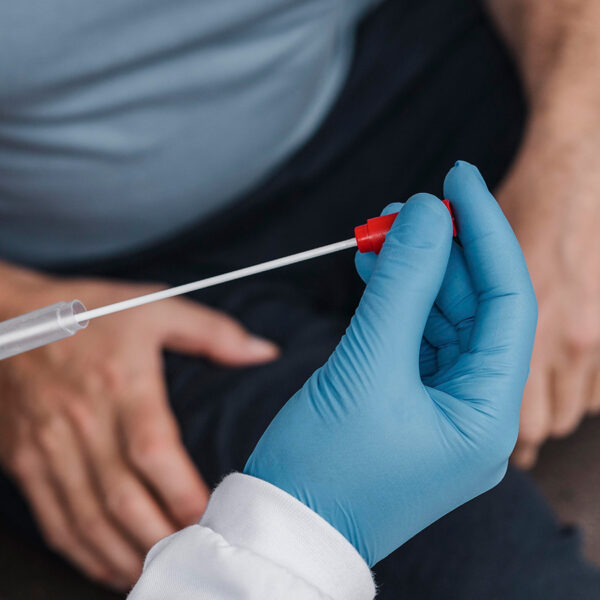
Spermograma
Este principalul test de evaluare a fertilității masculine și al succesului vasectomiei.
Recomandări recoltare:
- 3 zile abstinență (maxim 5)
- recoltare prin masturbare în recipient steril, prezervativ special sau coitus interruptus
- analiză în maximum 2 ore
- uneori 3 probe la interval de o săptămână
- în suspiciune obstructivă: PESA
Există kituri la domiciliu (din 2007), cu rezultate în 90 minute, precizie 95%, dar nu înlocuiesc evaluarea medicală.
Parametri analizați:
- Număr total: normal 30 milioane/ml; sub 20 milioane/ml = oligospermie; sub 100.000/ml = azoospermie.
- Motilitate (grade 1–4); normal >63% mobili sau minim 8 milioane mobili; fertilitate posibilă și la 50% cu mișcare adecvată.
- Morfologie: minim 12–14% forme normale poate fi suficient pentru fertilitate.
- Volum: normal 2,5–5 ml; sub 1 ml sugerează obstrucție; absență în ejaculare retrogradă; volume crescute pot cauza infertilitate.
- Fructoză: minim 300 mg/ml; valori scăzute sugerează obstrucție.
Biopsia testiculară
Indicată când se suspectează absența celulelor Sertoli, obstrucție tubulară sau spermatogeneză anormală cu hormoni normali. Se realizează sub anestezie generală, uneori bilateral. Riscuri: hemoragie, durere, lezarea epididimului. Se poate recurge la crioprezervare.
Analize obligatorii de screening
- HIV 1/2 (Ac + Ag p24)
- VDRL (RPR)
- TPHA
- Ac anti Treponema pallidum IgG/IgM
- Neisseria gonorrhoeae ADN
- Chlamydia trachomatis ADN
- Cultură micoplasme urogenitale
- Cultură secreție uretrală
- Cultură secreție vaginală
- HPV ADN (detecție + genotipare)
- Ac anti Herpes simplex 1+2 IgM
- Ag HBs (virus hepatic B)
- Examen bacteriologic (Trichomonas vaginalis)
Incidență, cauze diagnostic, tratament

În cadrul procedurilor de pregătire pentru fertilizare, ambii parteneri sunt supuși unor investigații și examene clinice detaliate. Diagnosticul de infertilitate a cuplului se stabilește doar după cel puțin un an de încercări de concepere, cu activitate sexuală normală, regulată și fără metode contraceptive. Totuși, dacă femeia are peste 35 de ani sau dacă oricare partener prezintă factori de risc, perioada de încercare se poate reduce semnificativ.
Evaluarea inițială include istoricul complet al pacientului, examenul fizic general și teste de laborator specifice. Realizată corect, această evaluare poate sugera cauza infertilității, poate confirma diagnosticul sau poate evidenția alte probleme medicale încă asimptomatice, cum ar fi mutații genetice, neoplazii sau diabet zaharat.
După investigații complexe și adesea îndelungate, se constată frecvent că femeia este sănătoasă. Abia ulterior bărbatul efectuează o spermogramă, care poate evidenția cauza infertilității, cum ar fi absența spermatozoizilor în spermă. Investigațiile masculine sunt mai simple și mai rapide, permițând un diagnostic și tratament mai prompt al infertilității.
Din acest motiv, în cazul infertilității de cuplu, se recomandă ca bărbatul să fie investigat primul, iar dacă spermograma este normală, să se continue evaluarea femeii.
În România nu există studii recente privind frecvența generală a infertilității și cea masculină. Studiile internaționale arată că în 6 din 10 cupluri care nu pot avea copii, cauza parțială sau totală este masculină. La bărbați, varicocelul, obstrucția căilor de eliminare a spermei, infecțiile urogenitale, bolile genetice și dezechilibrele hormonale pot afecta permanent calitatea spermei și pot duce la infertilitate.
Evaluarea începe cu discuția cu pacientul, urmată de examenul clinic pentru depistarea varicocelului, epididimitei, criptorhidiei sau obstrucției testiculare. Primul test efectuat este spermograma, care poate evidenția număr redus de spermatozoizi (oligospermie), absența lor completă (azoospermie), mobilitate redusă (astenospermie) sau structură anormală (teratospermie).
Pentru stabilirea cauzei exacte, se efectuează investigații suplimentare, inclusiv ecografie scrotală și transrectală a prostatei, dozări hormonale, cultură a spermei, teste pentru anticorpi antispermatici, dozarea fructozei spermatice, vasodeferentografie și teste genetice.
Tratamentul depinde de tipul de problemă. În cazul scăderii calității spermei, care poate include oligospermie, astenospermie, teratospermie sau combinații între acestea, varicocelul este o cauză frecventă și se tratează chirurgical prin varicocelectomie microscopică subinghinală, considerată procedura „gold standard”.
Alte cauze endocrine sau infecțioase se tratează medical. Dacă nu se identifică o cauză clară, pacienții sunt sfătuiți să renunțe la fumat, să adopte o dietă sănătoasă, să evite supraincalzirea organelor genitale și să aibă contacte sexuale regulate la două zile în apropierea ovulației. În cazul azoospermiei, aceasta poate fi obstructivă, când spermatozoizii se produc, dar nu sunt eliminați, sau neobstructivă, când testiculele nu produc suficienți spermatozoizi.
Tratamentul azoospermiei obstructive poate include procedura chirurgicală vasoepididimostomia prin invaginare, iar în azoospermia neobstructivă, recoltarea spermatozoizilor pentru fertilizare in vitro poate fi singura opțiune.
Cauze ale infertilității
Cauze generale
Infertilitatea masculină are multiple cauze, atât congenitale, cât și dobândite, iar prevalența acestora variază. Cele mai frecvente sunt vasectomia, varicocelul, infertilitatea idiopatică și azoospermia.
Vasectomia poate fi reversibilă prin vasovasostomie, dar apariția anticorpilor antispermatici poate limita succesul. Varicocelul reprezintă dilatarea venelor spermatice, afectând parenchimul testicular și reducând calitatea spermatozoizilor.
Lipsa celulelor Sertoli, fie congenitală, fie dobândită prin infecții sau expuneri toxice, perturbă spermatogeneza. Obstrucțiile tubilor seminiferi pot împiedica transportul spermatozoizilor. Vârsta influențează parametrii spermogramei, scăzând motilitatea și crescând anomaliile genetice.
Stresul fizic sau emoțional poate altera temporar numărul și mobilitatea spermatozoizilor. Activități precum sauna sau băile fierbinți reduc temporar fertilitatea. Consumul de droguri, alcool și fumatul afectează motilitatea și integritatea genetică a spermatozoizilor, iar obezitatea și malnutriția contribuie suplimentar.

Stil de viață și mediu
Parametrii spermogramei sunt influențați de factorii de mediu și stilul de viață. Stresul psiho-afectiv scade secreția de GnRH, afectând producția de spermatozoizi. Consumul cronic de alcool, droguri sau tutun diminuează motilitatea și durata de viață a spermatozoizilor.
Supraîncălzirea testiculelor, de exemplu prin saună sau băi fierbinți repetate, poate reduce temporar fertilitatea. Substanțele chimice din mediu, precum pesticidele, plumbul sau metalele grele, afectează funcția testiculară și hormonogeneza. Radicalii liberi produc stres oxidativ, distrug ADN-ul spermatozoizilor și reduc viabilitatea acestora.
Expunerea la substanțe estrogen-like sau ftalați poate compromite celulele Sertoli și procesele hormonale. Supravegherea mediului profesional și reducerea expunerii la toxine sunt esențiale pentru prevenirea infertilității. Temperaturile ridicate de la lenjeria strâmtă sau exerciții prelungite pot reduce producția de spermatozoizi.
Unele studii arată că fumătorii au libido mai scăzut și activitate sexuală mai redusă.
În general, stilul de viață și mediul înconjurător contribuie semnificativ la fertilitatea masculină.

Factori genetici
Infertilitatea masculină are adesea cauze genetice, care pot fi fie mostenite, fie dobândite. Anomaliile cromozomiale sau mutațiile în genele responsabile de spermatogeneză afectează calitatea și viabilitatea spermatozoizilor.
Aproximativ 10% din cazurile de infertilitate sunt asociate cu probleme ale acrozomului, care este esențial pentru penetrarea ovulului. Sindromul Klinefelter determină hipogonadism, microorhidism și infertilitate completă.
Fibroza chistică poate cauza absenta ductelor deferente și sterilitate la majoritatea pacienților. Sindromul Kartagener reduce motilitatea spermatozoizilor și duce frecvent la infertilitate. Rinichiul polichistic, prin chisturi în tractul reproducător, poate provoca infertilitate.
Spermatozoizii cu material genetic anormal sunt neviabili și pot crește riscul malformațiilor la descendenți. Testarea genetică ajută la identificarea riscurilor și la prevenirea transmiterii bolilor ereditare.
Terenul genetic și interacțiunea cu factorii de mediu explică de ce unii bărbați aparent sănătoși au până la 19% spermatozoizi anormali.

Boli, infecții și medicamente
Bolile sistemice și infecțiile pot compromite fertilitatea masculină. Diabetul, HIV, insuficiența renală sau hepatică și sindromul Cushing afectează producția de spermă.
Infecțiile genito-urinare, prostatitele și orhitele pot lăsa cicatrici ce blochează ductele spermatice. Infecțiile cu Chlamydia, gonoree sau HPV influențează negativ tubii seminiferi și motilitatea spermatozoizilor.
Oreionul post-pubertate poate deteriora testiculele în 25% din cazuri. Medicamentele precum steroizii anabolizanți, metotrexatul sau cimetidina afectează spermatogeneza și hormonogeneza.
Tratamentele hormonale, anticonvulsive și antipsihotice pot reduce calitatea spermei. Anticorpii antispermatici, frecvent post-vasectomie, pot distruge spermatozoizii sau împiedica fertilizarea.
Ejacularea retrogradă, provocată de traumatisme, boli sau medicamente, conduce la infertilitate.
Alte patologii, inclusiv siringomielia, traumatisme sau intervenții chirurgicale, completează lista cauzelor.

Anomalii anatomice
Anomaliile structurale afectează fertilitatea prin alterarea producției sau transportului spermatozoizilor. Varicocelul crește temperatura scrotului și afectează spermatogeneza, fiind prezent la 15–20% dintre bărbați.
Testiculul necoborât ridică temperatura locală, perturbă țesutul spermatogenic și crește riscul de cancer testicular. Hipospadiasul împiedică eliberarea spermatozoizilor și necesită corecție chirurgicală.
Obstrucția ductelor spermatice poate fi congenitală sau dobândită și blochează transportul spermatozoizilor. Anorhidia, lipsa completă a testiculelor, împiedică apariția caracterelor sexuale secundare.
Sindromul de disgenezie testiculară combină infertilitate, cancer testicular și malformații genitale. Traumatismele sau intervențiile chirurgicale majore pot afecta permanent structurile reproductive.
Evaluarea anatomiei scrotale și a ductelor este esențială pentru diagnostic și tratament. În anumite cazuri, corecțiile chirurgicale pot îmbunătăți fertilitatea.
Cancer și tratamente
Tratamentul cancerului poate afecta grav fertilitatea masculină. Rata concepțiilor după tratamente variază între 40 și 85%, în funcție de tipul și localizarea tumorii. Chimioterapia și radioterapia reduc calitatea și cantitatea spermatozoizilor și pot provoca infertilitate temporară sau permanentă.
Riscul crește dacă organele reproducătoare sunt aproape de zona iradiată. De obicei, spermatozoizii viabili lipsesc timp de aproximativ 5 ani, după care spermatogeneza se poate relua.
Crioprezervarea spermei înainte de tratament este recomandată pacienților tineri. Tratamentele moderne încearcă să reducă efectele adverse asupra sistemului reproducător.
Pentru băieții preadolescenți, cercetările vizează utilizarea celulelor stem pentru recapătarea fertilității fără risc de recidivă.
Monitorizarea pe termen lung a supraviețuitorilor este esențială. Educația și protecția fertilității fac parte din managementul holistic al cancerului, asigurând șanse mai mari de reproducere.

Ne poți suna sau poți completa și trimite formularul de mai jos
+40.256.488.466 – Recepție sau +40.723.246.199 – Dr. Tigaran Dan
